劉峰研究組發現血管微環境調控造血幹細胞發育的新機製
戰國時期,“孟母三遷”成就一代思想家孟子的典故可謂是家喻戶曉,這個故事向人們展示了環境因素的重要性。在生物體內,微環境同樣是造血幹細胞多步驟、多階段發育過程中不可或缺的因素。脊椎動物造血幹細胞產生於主動脈-性腺-中腎區,隨後遷移到胎肝(小鼠和人)或尾部造血組織(斑馬魚)進行擴增,進而遷移至胸腺向淋係分化,最後遷移至骨髓(小鼠和人)或腎髓(斑馬魚)以維持終生造血。由此可見,在造血幹細胞發育的不同階段,都有特定的微環境對其進行調控。其中,微環境如何調控造血幹細胞擴增成為該領域研究的熱點問題之一。
鑒於小鼠胚胎子宮內發育和部分突變體早期致死的局限性,中科院動物所劉峰研究員領導的血液與心血管發育研究組以斑馬魚為模式動物,重點研究和闡釋了尾部造血組織中血管內皮細胞對造血幹細胞擴增的作用及其機製。研究組充分利用斑馬魚體外發育和早期胚胎透明的優勢,通過激光共聚焦顯微鏡實時觀察,發現尾部造血組織處的造血幹細胞毗鄰於血管內皮細胞,並且其遷移和擴增具有尾部靜脈特異的方向性。這一現象暗示尾部血管內皮細胞是造血幹細胞微環境中的重要因素。通過對血管內皮細胞、造血幹細胞和尾部造血組織中其它細胞類群進行的全基因組表達譜分析,發現一個內皮細胞特異性的轉錄因子Klf6a。敲低或敲除klf6a會導致斑馬魚尾部造血組織中血管內皮所構成的微環境發生缺陷,從而阻礙了造血幹細胞的駐留和擴增。深入的分子機製探索發現,Klf6可以直接調控趨化因子ccl25b的表達,通過Ccl25b/Ccr7 趨化信號影響造血幹細胞擴增。另外,小鼠胎肝LSK細胞(Lin-Sca-1+c-Kit+)的體外培養實驗結果證明,該分子機製在高等哺乳動物胎肝造血中也是保守的。
上述工作揭示了造血微環境對造血幹細胞調控的新分子機製,發現Klf6a-Ccl25b/Ccr7信號軸介導造血幹細胞的擴增,同時也將為造血幹細胞的體外擴增和移植提供理論指導。該研究論文“The vascular niche regulates hematopoietic stem and progenitor cell lodgement and expansion via klf6a-ccl25b”於 2017年8月10日在線發表於Development Cell。
中科院動物所博士研究生薛媛媛為第一作者,劉峰研究員為通訊作者,該課題得到了國家傑出青年科學基金、國家自然科學基金重點項目、國家重點基礎研究發展計劃和中科院幹細胞與再生醫學戰略性先導科技專項的資助。(文章鏈接)
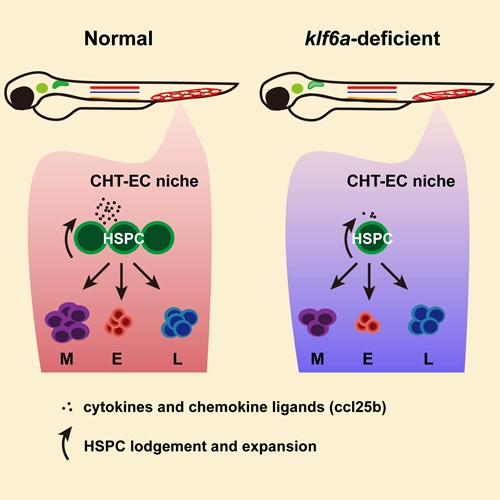
圖1:血管內皮細胞通過分泌重要的趨化因子調控造血幹細胞駐留和增殖。在正常個體中,斑馬魚尾部造血組織不僅為造血幹細胞提供物理性的生存環境,同時,血管內皮細胞可以通過分泌趨化因子吸引造血幹細胞在其中駐留以促進幹細胞的增殖。在klf6a缺陷的個體中,尾部血管的結構紊亂及血管內皮來源的趨化因子ccl25b的急劇減少,破壞了造血幹細胞寄居的微環境從而導致造血幹細胞在尾部造血組織的駐留和增殖能力下降。

圖2:“孟母三遷”的故事形象描繪了造血幹細胞(孟子)受微環境(孟母)誘導而遷移的曆程。圖中CHT(caudal hematopoietic tissue)表示尾部造血組織。

