魏妥團隊開發基於病毒融合肽的LNP遞送平台,實現mRNA高效胞內遞送
脂質納米顆粒(Lipid Nanoparticle,LNP)現已成為體內mRNA遞送的主流技術,在傳染病疫苗、蛋白替代療法、癌症治療及基因編輯等領域展現出了廣闊的應用前景。mRNA-LNP主要通過內吞途徑進入細胞,並被轉運到早期內體中。而mRNA需要從內體逃逸至細胞質中才能夠被翻譯成目的蛋白。然而,當前LNP的內體逃逸能力普遍不足,這嚴重製約了mRNA療法的治療效果。
2026年2月19日,必威精装版app西汉姆联 魏妥團隊在《Advanced Materials》(IF=26.8)上發表了題為“ Fusion Peptide-Incorporated Lipid Nanoparticles Boost Endosomal Escape and Enhance Cytosolic mRNA Delivery”的研究論文。該研究將具有兩親性的病毒來源或者人工合成的融合肽封裝於LNP內部,構建了基於融合肽的LNP(Fusion Peptide-LNP,FP-LNP)平台(圖1)。該方法顯著提升了LNP的遞送效率,其中,來源於流感病毒的HA2融合肽在體內外均表現出最優的mRNA遞送增強效果。機製研究表明,HA2的引入並未改變LNP的細胞攝取效率或體內器官分布,而是通過增強內體膜擾動能力和mRNA內體逃逸來提高mRNA-LNP的遞送效率。
研究團隊進一步考察了該策略的應用廣泛性:將HA2融合肽引入多種肝靶向LNP以及靶向肺髒和脾髒的器官靶向LNP(SORT LNP)中,均觀察到mRNA遞送效率的顯著提升。HA2-LNP共遞送Cas9 mRNA和sgTOM可以實現肝髒和肺髒中更高效的基因編輯。在遺傳性酪氨酸血症I型(HT-1)小鼠模型的蛋白替代療法研究中,與常規LNP相比,HA2-LNP更顯著地減輕了肝髒纖維化和炎症浸潤,表現出了顯著的治療優勢。
該研究通過將病毒融合肽引入mRNA-LNP,成功開發了一種普適而高效的策略來突破mRNA療法的內體逃逸瓶頸。該平台不僅與現有多種LNP配方兼容,且在基因編輯和蛋白替代療法中展現出增強的治療潛力,為下一代高效mRNA藥物的開發提供了新的思路。
必威精装版app西汉姆联 魏妥研究員為該論文的通訊作者,必威精装版app西汉姆联 博士研究生蒙亞楠為第一作者。該研究得到了中國科學院戰略性先導專項、國家自然科學基金等項目資助。
文章鏈接:https://doi.org/10.1002/adma.202515130

圖1. 病毒融合肽提高mRNA-LNP的內體逃逸和遞送效率
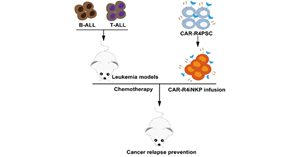
CAR-NK細胞在疾病治療中展現出安全和通用的優勢,但療效不理想。臨床上,為了提高CAR-NK細胞療效,多采用高劑量、多劑次輸注給藥的策略,這導致治療成本顯著增加,加重患者經濟負擔。因此,傳統的人體組織來源CAR...
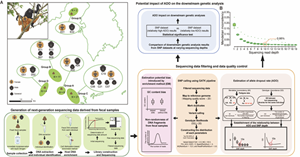
海南長臂猿(Nomascus hainanus)是全球最稀有靈長類,被列為國家一級重點保護野生動物,國際自然保護聯盟(IUCN)物種紅色名錄“極危(Critically Endangered)”物種,也是海南熱帶雨林國家公園的旗艦物種。受...
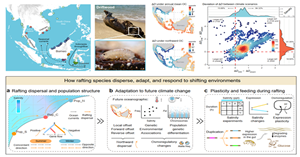
漂流擴散(Rafting dispersal)被認為是海洋物種在氣候變化驅動下追蹤適生生態位的重要方式。然而,物種如何在跨越漫長距離的漂流過程中,適應海洋環境波動以及應對未來氣候變化,仍然缺乏深入了解。

