必威在线网址 合作揭示核纖層蛋白塑造三維基因組空間秩序的機製
人類基因組總長度近2米,卻能在直徑僅約10微米的細胞核內高度有序地折疊,其壓縮尺度相當於將珠穆朗瑪峰高度的精細模型裝入一枚乒乓球中,這是生命科學中最令人驚歎的現象之一。基因組的有序性體現在多層次的三維構象上,包括大尺度的染色體疆域和A/B區室,以及更小尺度的拓撲相關結構域(topologically associating domains,TADs)和染色質環(chromatin loops)。單個染色體及其結構域在核內的偏好性定位也遵循特定的空間規律:轉錄抑製的異染色質通常富集於核周,而轉錄活躍的常染色質則傾向定位於核內。與之相呼應的是,負責轉錄激活和RNA加工的核斑(nuclear speckle)也通常分布於核內。這些精密的空間結構使得細胞能夠在不同發育階段實現基因表達的精準調控。因此,闡明基因組空間組織的形成與調控機製,已成為領域內的核心科學問題。
核纖層(nuclear lamina)是緊貼內核膜內側的蛋白網狀結構,主要由核纖層蛋白(lamins)及其結合蛋白構成。在人類中,lamins分為A型(由LMNA基因編碼)和B型(分別由LMNB1和LMNB2編碼)。Lamins在發育、衰老與疾病過程中扮演關鍵角色,目前已在LMNA基因中鑒定出超過600種致病突變,可導致包括兒童早衰症和擴張型心肌病在內的多種核纖層病(laminopathies)。傳統上,核纖層病的病因被主要歸結為細胞核機械穩定性的下降。與核纖層相互作用的大尺度基因組區域被稱為核纖層相關結構域(lamina-associated domains,LADs),盡管LADs的核周定位被認為依賴於其與核纖層的相互作用,但不同lamins成員在此過程中的具體功能分工,以及它們如何協同維持正常與病理狀態下的染色質高級結構,仍有待係統闡明。
研究團隊在核纖層疾病領域的探索始於2011年。彼時,他們率先利用兒童早衰症患者的細胞成功構建了誘導多能幹細胞,發現表觀遺傳重編程可以逆轉細胞核的衰老特征,這為在細胞層麵探索“衰老逆轉”提供了早期證據(Nature 2011)。隨後,團隊利用第三代腺病毒載體技術,在患者幹細胞中成功實現了對LMNA致病突變的精準矯正,這項工作為基於基因編輯的原位治療策略提供了重要的概念驗證(Cell Stem Cell 2011)。此後,通過結合HDAdV與TALEN技術,團隊開發了更安全高效的telHDAdV基因編輯係統(Cell Stem Cell 2014)。基於這些技術積累,他們與合作者陸續創建了攜帶LMNA突變的兒童早衰症胚胎幹細胞及非人靈長類疾病模型(Cell 2016,Protein Cell 2018/2020),並係統揭示了核纖層異常導致多維表觀基因組重塑及古病毒複活的規律(Dev Cell 2022,Cell 2023, Cell Reports 2023)。這些持續而係統的前期工作,為本次深入揭示lamins在三維基因組中的核心功能奠定了堅實基礎。
基於團隊在核纖層病研究研究領域的多年積累,近日,必威精装版app西汉姆联 曲靜研究組、劉光慧研究組與中國科學院北京基因組研究所張維綺課題組合作,在Cell Reports雜誌發表了題為“Nuclear-lamin-guided plastic positioning and folding of the human genome”的研究論文。該研究揭示了“基因組積木模型”的幕後搭建者—lamins在人類幹細胞三維基因組結構中的關鍵角色,首次係統繪製了lamins家族缺失下的人類三維表觀基因組全景圖譜,並證明了lamins不僅是基因組–核纖層錨定及大尺度基因組結構的關鍵調控者,還通過與核斑結構蛋白SON的相互作用,精確調控核斑的空間定位與聚集。該研究將核纖層病的病理機製認知從傳統的“細胞核機械性脆弱”模型,推動至“三維基因組組織紊亂導致基因表達失調”的新範式,為深入理解核纖層病的發病機製提供了全新視角。
首次係統繪製lamins家族擾動的人類三維基因組圖譜
研究首次在人正常二倍體細胞中實現了lamins家族的係統性敲除。在人胚胎幹細胞中(human embryonic stem cells,hESCs),lamins缺失未顯著影響幹細胞穩態;然而,在人間充質幹細胞中(human mesenchymal stem cells,hMSCs),B型lamins缺失導致核膜起泡,而lamin A/C/B1/B2全敲除(triple knockout,TKO)則引起嚴重的核形變,導致約70%的LAD脫離核周,甚至改變了染色體的定位偏好,並伴隨細胞增殖能力的顯著下降。研究進一步通過整合多達14個維度的表觀基因組數據,並結合基因組熒光原位雜交技術,突破了以往研究多依賴於單一技術層麵的局限,革新了領域內對基因組-核纖層錨定模型的認知。
修正人類基因組–核纖層錨定模型
研究根據基因組對lamins的依賴程度,建立了一套全新的基因組–核纖層錨定模型:L1區域(富集A/T序列且缺乏經典組蛋白修飾)依賴於全部lamins的共同錨定,在TKO後完全脫離核周;L2區域(富集H3K9me3修飾)由lamins與lamin B受體(lamin B receptor,LBR)共同錨定,僅在TKO中進一步敲除LBR的條件下才脫離核周;L3區域(富集H3K27me3修飾且位於LAD邊界)對lamins缺失極為敏感,在單/雙敲除條件下即發生脫離。進一步分析發現,不同亞型的inter-LAD(iLAD)—iL1、iL2和iL3—在lamins缺失後也遵循不同的轉變規律:iL1區域(富集啟動子狀態和轉錄活躍的核斑)僅在TKO後從核內翻轉至核周;iL2區域(富集增強子狀態)在TKO後仍位於核內;iL3區域(富集鋅指蛋白基因且位於iLAD邊界)在單/雙敲除條件下即發生核內向核周翻轉。這表明lamins不僅負責將LAD錨定於核周,對於維持特定基因組區域在核內的定位也發揮著關鍵作用。
Lamins維持人類大尺度三維基因組結構
研究填補了領域內對基因組大尺度空間組織機製的認知空白,提出lamins是大尺度三維基因組結構的關鍵組織者,包括染色體疆域、染色質區室互作簇(A–A和B–B)以及跨度達10 Mb以上的mega-loops結構。值得注意的是,局部染色質結構(如TADs和loops)及其組織因子CTCF/cohesin的結合模式在lamins缺失時基本得以保留。這提示可能存在兩種不同的組織原則分別調控大尺度構象(lamins)與局部構象(CTCF/cohesin)。研究提出,lamins作為關鍵的結構支架,通過限製LAD之間的接觸以維持染色體疆域的隔離,並通過維持染色體內的長程互作簇來促進染色質的壓縮。
核斑組織紊亂及核纖層病的機製見解
研究證實lamin A與核斑支架蛋白SON之間存在相互作用。Lamins缺失導致核斑和iL1富集的核斑結構域(speckle-associated domains,SPADs)從核內翻轉至核周,其空間聚集也被破壞,這一係列結構變化引發了全局性轉錄水平下調。超過75%的下調基因定位於SPADs,並富集於細胞周期通路,其中生長調控轉錄因子EGR1的抑製最為顯著,這直接損害了細胞的增殖能力。該發現將幹細胞功能障礙置於核纖層病發病機製的核心位置,提示成體幹細胞耗竭可能是驅動組織退化和早衰的關鍵因素。重新表達野生型lamin A可部分恢複基因組層級結構、核斑分布與轉錄水平,而與核纖層病相關的E161K突變體則基本喪失了恢複能力。這些結果不僅揭示了lamins在細胞核空間結構中的多層次調控作用,更首次直接將“核斑錯誤定位”與“核纖層病”聯係起來,為闡明lamins功能障礙的致病機製提供了關鍵的分子解釋。
綜上所述,該研究在hESCs及其分化來源的hMSCs中首次構建了lamins的單、雙、三敲除模型,係統揭示了lamins在基因組徑向定位與空間折疊中的核心作用。與hESCs不同,hMSCs對lamins缺失異常敏感,表現出嚴重的核形變及大規模的空間基因組重構。其核心機製在於,lamin A通過與SON的相互作用來維持核內結構,而致病突變E161K則會破壞此過程。該研究的意義不僅限於典型的核纖層病:鑒於細胞衰老普遍伴隨核纖層紊亂,此發現為理解生理性衰老及防治衰老相關疾病提供了重要的新線索和潛在靶標。這項工作不僅揭示了核纖層病的潛在機製,更將相關疾病的病理認知推向了一個統一的“三維基因組紊亂”框架,為未來開發靶向lamin-SON軸的治療策略奠定了理論基礎。
必威精装版app西汉姆联 王澤華博士、季乾昭博士、劉尊鵬博士和博士研究生焦春雨為該研究的並列第一作者。必威精装版app西汉姆联 曲靜研究員、劉光慧研究員和國家生物信息中心(中國科學院北京基因組研究所)張維綺研究員為該研究的共同通訊作者。該研究得到中國科學院深圳先進技術研究院曹罡教授的指導與支持。
原文鏈接:https://doi.org/10.1016/j.celrep.2025.116529

圖:核纖層蛋白家族協同錨定染色質和核斑維持人類三維基因組結構
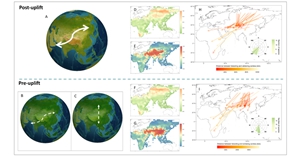
青藏高原隆升是地球曆史上最重要的地質事件之一,不僅塑造了亞洲大陸的地形格局,也深刻影響了區域氣候與生態係統的演化。
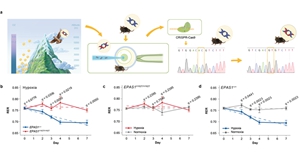
機體通過自我調節來維持內環境的穩定是生命的一般原則,被稱為穩態。在麵對外界環境壓力時,機體穩態的維持需要能量供應,這些能量主要源於新陳代謝(底物主要為糖和脂)。低氧是青藏高原生物麵臨的主要環境脅迫...

